
- Tiếng Việt
- English
Nghiên cứu chiết xuất Sulforaphane từ súp lơ xanh bằng phương pháp chiết xuất pha rắn
Quá trình thủy phân glucoraphanin tạo ra nhiều loại hợp chất (glucose, sulfate, isothiocyanates, thiocyanates, nitriles) gây cản trở quá trình tách và xác định sulforaphane. Do đó, cần thiết phải thiết lập một phương pháp đơn giản và thuận tiện cho việc chiết tách sulforaphane từ súp lơ xanh.
Trong nghiên cứu này, sự ảnh hưởng của các chất thủy phân khác nhau tới quá trình chiết xuất sulforaphane đã được loại bỏ bằng cách lựa chọn pH tối ưu và ba loại cột sắc ký (cartridges) chiết pha rắn khác nhau được sử dụng để tinh chế sulforaphane.
1. Nghiên cứu tối ưu hóa các điều kiện sắc ký
Lựa chọn các điều kiện HPLC tối ưu rất quan trọng đối với việc xác định và tách suforaphane. Trong nghiên cứu này, các bước sóng khác nhau (205 nm, 235 nm và 254 nm) đã được nghiên cứu và kết quả cho thấy sulforaphane có độ hấp thụ lớn nhất ở bước sóng 205nm. Do đó, bước sóng 205nm đã được chọn để phân tích thêm.
Các loại pha động khác nhau như methanol, acetonitril và nồng độ khác nhau của methanol / H2O và acetonitrile / H2O đã được nghiên cứu. Dưới 205nm, metanol có độ hấp thụ nền mạnh, rất khó để cân bằng cột C18.
Trong khi đó hệ dung môi Acetonitrile và H2O tỷ lệ 1:4 (thể tích/thể tích) đã được chứng minh là mang lại sự phân tách tốt nhất, vì không có sự can thiệp của các tạp chất khác và thời gian lưu của sulforaphane là ngắn. Sắc ký đồ của sulforaphane được thể hiện trong hình dưới đây.
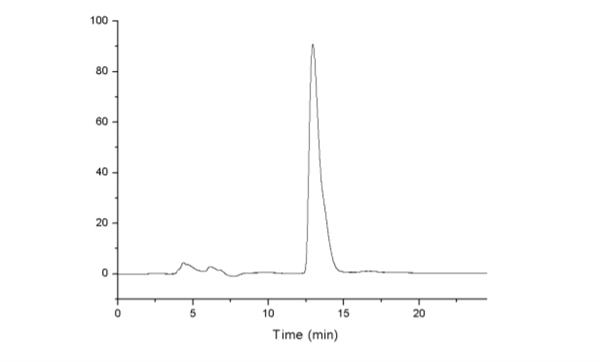
Sắc kỳ đồ chuẩn của sulforaphane với pha động là acetonitrile/water (tỷ lệ 20/80), thể tích chất tiêm vào là 10µl, bước sóng 205 nm
1.1. Tối ưu hóa quá trình thủy phân từ Glucoraphanin thành Sulforaphane
Để tối ưu hóa quá trình thủy phân glucoraphanin thành sulforaphane trong bông cải xanh tươi (súp lơ xanh), thử nghiệm sơ bộ được tiến hành với độ pH khác nhau của dung dịch axit (3, 4, 5 và 6) và thời gian thủy phân (2, 4 và 6 giờ), nhiệt độ ủ không đổi ở 35 ° C.
Bảng 1 cho thấy sulforaphane thu được lượng cao nhất với pH 3.0 và thời gian thủy phân 4 giờ.
| pH | Lượng Sulforaphane thu được sau khi chiết xuất (mg/g) |
| 0 | 0.024 |
| 2.0 | 0.057 |
| 3.0 | 0.148 |
| 4.0 | 0.132 |
| 6.0 | 0.118 |
1.2. Tối ưu hóa các điều kiện chiết xuất pha rắn
Lựa chọn chất nhồi cột khác nhau
Trong nghiên cứu này, ba loại cột chiết xuất pha rắn khác nhau (C18, amino và silica) đã được sử dụng và lượng rửa giải với các dung môi khác nhau được thể hiện trong Bảng 2.
Những dữ liệu này cho thấy cột nhồi silica tốt hơn hơn hai loại cột còn lại để chiết xuất sulforaphane. Điều này có thể được giải thích là do sự phân cực yếu của sulforaphane, được hấp thụ dễ dàng bởi một cột phân cực yếu.
Bảng 2: Lượng sulforaphane chiết xuất được khi sử dụng các dung môi khác nhau trong quá trình rửa và với các pha tĩnh khác nhau.
| Loại dung môi | Hàm lượng sulforaphane (mg/g) | ||
| Cột nhồi Silica | Cột nhồi C18 | Cột nhồi Amino | |
| Nước | 0.016 | 0.003 | 0.002 |
| Acetonitrile | 0.069 | 0.032 | 0.027 |
| Dichloromethane | 0.357 | - | 0.057 |
| Acetic acid 0.1M | - | 0.062 | - |
| Hexane | - | - | 0.006 |
| Ethyl acetate | 0 | 0 | - |
Lựa chọn dung môi rửa cột và rửa giải thích hợp
Trong chiết xuất pha rắn, lựa chọn dung môi rửa giải thích hợp yếu tố được quan tâm hàng đầu bởi vì nó có ảnh hưởng trực tiếp đến hiệu quả chiết xuất.
Đối với các dung môi rửa giải phân cực (nước, acetonitril, dichloromethane và ethyl acetate) đã được nghiên cứu.
Bảng 2 cho thấy sulforaphane không được rửa sạch bởi ethyl acetate. Do đó, ethyl acetate được chọn làm dung môi rửa thích hợp. Hơn nữa, sulforaphane có thể là rửa sạch đồng thời với một lượng lớn các hợp chất không cần thiết khi nước, acetonitril, và dichloromethane đã được sử dụng.
Trong đó lượng sulforaphane tương đối lớn nhất đã được dichloromethane rửa sạch. Do đó, dichloromethane được sử dụng làm dung môi rửa giải trong bước tiếp theo
Bên cạnh đó, thể tích dung môi rửa giải là một trong những yếu tố khác cần được xem xét. Một loạt các thí nghiệm đã được tiến hành để nghiên cứu sự thay đổi thể tích của dung môi rửa giải tới lượng chất chiết xuất được
Kết quả thu được trong bảng 3, có thể thấy rằng lượng chiết xuất sulforaphane tăng lên với thể tích dichloromethane tăng từ 2 đến 6 ml. Khi thể tích diclometan vượt quá 4 ml thì lượng sulforaphane gần như không đổi. Do đó, dựa trên kết quả thí nghiệm này thì thể tích dichloromethane là 4 ml đã được lựa chọn.
| Thể tích dichloromethane (ml) | Lượng sulforaphane (mg/g) |
| 2 | 0.120 |
| 3 | 0.214 |
| 4 | 0.324 |
| 5 | 0.326 |
| 6 | 0.27 |
Bảng 3: Nghiên cứu thể tích dichloromethane thích hợp cho chiết xuất sulforaphane
2. Tiến hành chiết xuất
Sau đây, mời bạn cùng tìm hiểu phương pháp chiết xuất sulforaphane bằng phương pháp chiết pha rắn.
2.1. Chuẩn bị nguyên liệu và thuốc thử
Sulforaphane được mua từ công ty hóa chất Sigma-Aldrich (Hoa Kỳ), thuộc sở hữu của Merck KGaA và được sử dụng mà không cần tinh chế thêm.
Các loại dung môi Acetonitril, metanol, ethyl acetate và dichloromethane được sản xuất bởi Công ty TNHH Duksan Pure Chemical (Ansan, Hàn Quốc).
Các dung dịch chuẩn của sulforaphane đã được điều chế bằng cách hòa tan 10 mg chất chuẩn trong 10 ml acetonitril.
Các cột sắc ký C18, amino và silica (200 mg/3 mL) đã được mua từ Alltech (Hoa Kỳ).
Việc phân tách sulforaphane thông qua HPLC được tiến hành bằng cách sử dụng acetonitril/H2O (với tỷ lệ 20/80) làm pha động với tốc độ dòng 0,5 ml/phút và được thực hiện ở bước sóng 205nm. Nước cất được lọc bằng bơm chân không và bộ lọc (HA-0,45 m; Millipore, Waters, USA) trước khi sử dụng.
2.2. Làm sạch mẫu và chuẩn bị chiết xuất
Súp lơ xanh tươi được nghiền thành bột, cân 5 g bột và chiết xuất với 20 ml dung dịch axit clohydric (HCl) với các pH khác nhau trong 2 giờ. Hỗn hợp thu được tiếp tục được chiết xuất 3 lần với 20 ml dichloromethane, sau đó thêm natri sunfat khan để hút nước.
Phần dichloromethane được sấy khô ở 30 ° C trong chân không. Các cặn được hòa tan trong acetonitril và sau đó được lọc qua bộ lọc màng 0,22 mm cho nghiên cứu sau.
Sau đó, sulforaphane sẽ được tinh chế với các loại cột khác nhau. Trước khi sử dụng, các cột pha tĩnh chứa silica được điều hòa với 4 mL dichoromethane, cột pha tĩnh C18 được điều hòa với 4 ml metanol và cột pha tĩnh amino được điều hòa với 4 mL ethyl acetate.
Đầu tiên, 200 μL chiết xuất hữu cơ được nạp qua ba loại hộp mực khác nhau, sau đó hộp silica được rửa bằng 4,0 ml etyl axetat (sau đó được loại bỏ) và sulforaphane rửa giải bằng 4 ml dichloromethane.
Cột pha tĩnh C18 được rửa bằng 4 mL nước (sau đó đã bị loại bỏ) và sulforaphane rửa giải bằng 4 ml axit axetic 0,1 mol/l; và hộp mực amino được rửa với 4ml ethyl acetate (sau đó đã bị loại bỏ) và sulforaphane rửa giải với 4 mL diclometan.
Các chất chiết thu được được làm bay hơi đến khô trong tủ hút chân không ở 45 ° C trong 2 h và được hòa tan với 2 mL acetonitril.
10 μL mẫu của các dung dịch này sau đó được tiêm vào cột của hệ thống HPLC. Tất cả các mẫu được phân tích thành hai bản
Kết quả thu được lượng sulforaphane được chiết xuất từ súp lơ xanh là 0,513 mg/g.
Mong rằng qua những thông tin mà bài viết đã cung cấp đã giúp các bạn có thêm nhiều thông tin về phương pháp chiết xuất Sulforaphane.
Tài liệu tham khảo
http://cyber.sci-hub.tw/MTAuMzM5MC9pam1zMTIwMzE4NTQ=/10.3390%40ijms12031854.pdf














Viết bình luận